ホーム> 政策について> 分野別の政策一覧> 健康・医療> 食品> 食品添加物> よくある質問 (事業者向け)
よくある質問 (事業者向け)
Q1.食品添加物が使用できるかどうかを確認したいのですが?
(1) 使用できる添加物の品目について
日本で使用が可能な添加物は、指定添加物、既存添加物、天然香料、一般飲食物添加物です。
 品目一覧はこちら
品目一覧はこちら
(2) 添加物の規格について
(3) 使用が可能な食品について
食品添加物には使用基準(使用上限量、対象食品など)が定められているものがあり、その使用基準の範囲内において使用が認められています。
 詳細はこちら
詳細はこちら
なお、食品添加物の食品への使用にあたってご不明な点がありましたら、お近くの保健所又は検疫所輸入相談窓口へお問い合わせください。
<参考>
 検疫所輸入相談窓口一覧
検疫所輸入相談窓口一覧
Q2.食品添加物の指定や規格基準の改正はどのような手続きが必要ですか?
食品添加物の指定又は規格基準の改正(以下「指定等」という。)には、(1)内閣府食品安全委員会の安全性の評価(食品健康影響評価)と(2)厚生労働省の審議(規格基準案の検討等)等が必要です。
なお、指定等に必要な資料は、指定を要請する事業者が自ら収集し、厚生労働省に提出する必要があります。
具体的に必要な資料や記載方法は、指定等要請資料の手引、内閣府食品安全委員会が作成したガイドラインを参考にしてください。
 詳細はこちら
詳細はこちら
- <指定等要請資料の手引>
 食品添加物の指定及び使用基準改正要請資料作成に関する手引[PDF] [759KB](平成26年9月厚生労働省医薬食品局食品安全部基準審査課)
食品添加物の指定及び使用基準改正要請資料作成に関する手引[PDF] [759KB](平成26年9月厚生労働省医薬食品局食品安全部基準審査課) 別添資料(別添1~3、チェックリスト)[Word] [35KB]
別添資料(別添1~3、チェックリスト)[Word] [35KB] 食品添加物の指定及び使用基準改正に関する指針について[PDF] [266KB](平成8年3月(令和4年9月改正)厚生労働省医薬・生活衛生局食品基準審査課)
食品添加物の指定及び使用基準改正に関する指針について[PDF] [266KB](平成8年3月(令和4年9月改正)厚生労働省医薬・生活衛生局食品基準審査課) 香料の指定に関する指針について[PDF] [142KB](平成28年5月厚生労働省医薬・生活衛生局生活衛生・食品安全部基準審査課)
香料の指定に関する指針について[PDF] [142KB](平成28年5月厚生労働省医薬・生活衛生局生活衛生・食品安全部基準審査課) 「添加物に関する食品健康影響評価指針」の改正等及び添加物の指定等の要請書に添付すべき資料について[PDF] [61KB](平成29年7月厚生労働省医薬・生活衛生局食品基準審査課)
「添加物に関する食品健康影響評価指針」の改正等及び添加物の指定等の要請書に添付すべき資料について[PDF] [61KB](平成29年7月厚生労働省医薬・生活衛生局食品基準審査課)- <内閣府食品安全委員会が作成したガイドライン>
 添加物に関する食品健康影響評価指針[PDF] [764KB](2010年5月食品安全委員会決定,2017年7月改正、2021年9月改正)
添加物に関する食品健康影響評価指針[PDF] [764KB](2010年5月食品安全委員会決定,2017年7月改正、2021年9月改正) 香料に関する食品健康影響評価指針[PDF] [1518KB](2016年5月食品安全委員会決定、2021年9月改正)
香料に関する食品健康影響評価指針[PDF] [1518KB](2016年5月食品安全委員会決定、2021年9月改正) 添加物(酵素)に関する食品健康影響評価指針[PDF] [464KB](2017年7月食品安全委員会決定、2021年9月改正)
添加物(酵素)に関する食品健康影響評価指針[PDF] [464KB](2017年7月食品安全委員会決定、2021年9月改正) 栄養成分関連添加物に関する食品健康影響評価指針[PDF] [594KB](2017年7月食品安全委員会決定、2021年9月改正)
栄養成分関連添加物に関する食品健康影響評価指針[PDF] [594KB](2017年7月食品安全委員会決定、2021年9月改正)- <標準的事務処理期間>
 食品添加物の指定等手続に係る標準的事務処理期間の設定について[PDF] [152KB](平成28年6月厚生労働省医薬・生活衛生局生活衛生・食品安全部基準審査課)
食品添加物の指定等手続に係る標準的事務処理期間の設定について[PDF] [152KB](平成28年6月厚生労働省医薬・生活衛生局生活衛生・食品安全部基準審査課)
また、平成26年7月より、指定等要請者からの事前相談等の一部の業務については、国立医薬品食品衛生研究所の食品添加物指定等相談センター(Food Additive Designation Consultation Center)において実施することとなりましたので、食品添加物の指定等にあたり、ご活用ください。
 食品添加物指定等相談センター
食品添加物指定等相談センター
<食品安全委員会の設置前に厚生労働省が作成した評価指針>
 食品添加物の指定及び使用基準改正に関する指針について※この指針は令和4年9月に改正しました。改正後の指針は<指定等要請資料の手引き>に掲載しています。
食品添加物の指定及び使用基準改正に関する指針について※この指針は令和4年9月に改正しました。改正後の指針は<指定等要請資料の手引き>に掲載しています。
 保健機能食品であってカプセル、錠剤等の通常の食品形態ではない食品の成分となる物質の指定及び使用基準改正に関する指針について
保健機能食品であってカプセル、錠剤等の通常の食品形態ではない食品の成分となる物質の指定及び使用基準改正に関する指針について
連絡先
医薬・生活衛生局食品基準審査課添加物係(内線2453)
<食品添加物の指定等に関する手続き>
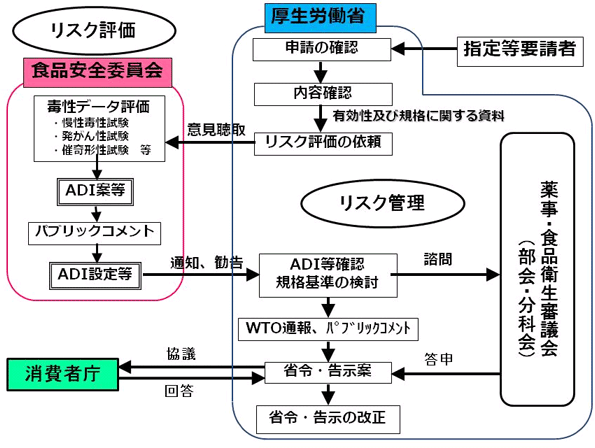
<必要な資料一覧>
(添加物に関する食品健康影響評価指針(2017年7月食品安全委員会)より抜粋)
| 項目 | 指定 | 基準改正 | ||
|---|---|---|---|---|
| 評価対象添加物の概要 | 1 名称及び用途 | ○ | ○ | |
| 2 起源又は発見の経緯 | ○ | △ | ||
| 3 諸外国における使用状況 | ○ | ○ | ||
| 4 国際機関等における評価 | ○ | △ | ||
| 5 物理化学的性質 | ○ | △ | ||
| 6 使用基準案 | ○ | ○ | ||
| 7 その他 | △ | △ | ||
| 安全性に係る知見 | 1 体内動態試験 | ○ | △ | |
| 2 毒性 | (1)亜急性毒性試験及び慢性毒性試験 | ○ | △ | |
| (2)発がん性試験 | ○ | △ | ||
| (3)1 年間反復投与毒性/発がん性併合試験 | ○ | △ | ||
| (4)生殖毒性試験 | ○ | △ | ||
| (5)出生前発生毒性試験 | ○ | △ | ||
| (6)遺伝毒性試験 | ○ | △ | ||
| (7)アレルゲン性試験 | ○ | △ | ||
| (8)一般薬理試験 | ○ | △ | ||
| (9)その他の試験 | △ | △ | ||
| 3 ヒトにおける知見 | ○ | △ | ||
| 4 一日摂取量の推計等 | ○ | ○ | ||
- (注1)食品安全委員会による食品健康影響評価の行われた添加物の使用基準改正に当たっては、「基準改正」の資料を提出すること。一方、食品安全 委員会による食品健康影響評価のなされていない添加物については、原則として添加物の指定のための評価に必要とされる資料を提出する。
- (注2)○印は添付すべき資料。△印は新たな知見がある場合等必要な場合に添付すべき資料を示す。
- (注3)慢性毒性/発がん性併合試験をげっ歯類1種について実施した場合には、慢性毒性試験及び発がん性試験のげっ歯類1種についての試験を省略することができる。
PDFファイルを見るためには、Adobe Readerというソフトが必要です。Adobe Readerは無料で配布されていますので、左記のアイコンをクリックしてダウンロードしてください。

